
L’arrivée des psychotropes a bouleversé le paysage de la psychiatrie. Si le bénéfice que l’industrie retire de cette mutation est imposant, celui qui revient aux patients est beaucoup plus incertain…
Historique
Après la seconde guerre mondiale s’est renforcé, de part et d’autre de l’Atlantique, un mouvement visant à réduire l’internement des malades mentaux et à promouvoir le développement de projets communautaires, véritables alternatives à l’hospitalisation psychiatrique1. L’arrivée de nouveaux médicaments psychotropes quelques années plus tard a suscité de grands espoirs pour l’amélioration des soins en pathologie mentale, que ce soit dans ou hors des hôpitaux. Cet enthousiasme a légitimement trouvé sa source dans l’effet réel et rapide de soulagement de certains patients. Les méthodes thérapeutiques comprenaient jusque-là des traitements de choc, des traitements physiques, de la psychochirurgie ou des thérapies interpersonnelles longues. La pratique de ces dernières était d’acquisition difficile, leurs théories pouvaient paraître réservées à une élite d’initiés et critiquables sur le plan scientifique2. Avec la psychiatrie biologique, la psychiatrie espérait retrouver le champ clair et limpide de la médecine : une maladie = un traitement = la guérison. Mais ce faisant, elle rejetait dramatiquement dans l’ombre la réalité de la pratique de la clinique médicale, psychothérapeutique ou psychiatrique, qui est celle de la chronicité, du traitement pluridisciplinaire, de l’engagement humain au long cours auprès du patient, avec ou sans l’aide de psychotropes. La psychiatrie s’est orientée dans les décennies suivantes vers un modèle explicatif des patholo gies impliquant une anomalie du cerveau, un déséquilibre des neurotransmetteurs, en remon tant à contresens le lien entre la pathologie et le traitement médicamenteux. Ce qui donne, par exemple, pour la dépression : « si un médica ment agit sur la dépression en modifiant le taux de sérotonine ALORS la dépression est causée par un déficit en sérotonine ». Relation absurde puisqu’elle reviendrait à dire que « si une céphalée est améliorée par l’acide acétylsalicylique ALORS cette céphalée est causée par un déficit en acide acétylsalicylique »3. Une autre généralisation abusive concerne la dopamine4. Celle- ci intervient dans le cerveau du rat dans la prise de décision pour obtenir une récompense et est présentée depuis quelques années comme « la molécule du plaisir ou de la motivation ». Ce slogan n’a qu’une correspondance simpliste avec la réalité neurobiologique. Il incite à penser que toute perte de motivation est pathologique et serait du ressort de la médecine (dépression, trouble déficitaire de l’attention avec hyperactivité, consommation de cannabis, adolescence, ménopause, retraite…). Les faiblesses des hypothèses étiologiques de la psychiatrie biologique qui se révèlent en réalité n’être rien de plus que des arguments commerciaux ou des effets de mode dans les milieux scientifiques mériteraient de plus amples développements mais ne sont cependant pas l’objet de la présente réflexion. Quand nous utilisons le terme « dérive », de quoi s’agit-il ? Quelle en est l’ampleur ? Prenons le cas des antidépresseurs. Dans deux rapports récents, nous observons en Belgique comme en France le même profil de surconsommation5, 6 : le volume de consommation a quasiment doublé en moins de dix ans ; les femmes consomment davantage que les hommes ; les personnes âgées sont les plus concernées mais toutes les tranches d’âge sont affectées par cette extension (jeunes enfants y compris). 85% des prescriptions proviennent des médecins généralistes et font souvent suite à un bref entretien. Deux faits inquiétants méritent d’être soulignés. Premièrement, les médicaments psychotropes manqueraient leur cible. En effet, la plupart de ceux qui bénéficient de traitements remboursés seraient finalement atteints de troubles existentiels passagers ou à résolution spontanée alors que les mélancoliques nécessitant des traitements psychiatriques seraient eux laissés sans soins. Deuxièmement, d’après le rapport annuel de l’Organe international de contrôle des stupéfiants publié le 1er mars 2007, l’abus et le trafic de médicaments psychotropes délivrés sur ordonnance mais consommés en dehors de tout contrôle médical seraient en train de dépasser ceux des drogues illicites7. Il n’est pas possible de trouver une responsabilité unique des uns ou des autres dans cette situation. Il y a bien sûr, comme dans les autres disciplines médicales, la pression commerciale des firmes pharmaceutiques. Nous sommes nombreux8 à déplorer la surreprésentation de ces firmes dans tous les lieux stratégiques (universités, hôpitaux, agences de régulation, commissions de remboursement,…), engendrant des conflits d’intérêts généralisés, ainsi que leur maîtrise complète de tous les rouages de l’information médicale (information et formation des médecins, soutien d’associations de patients, « informations » sur les maladies dans les médias,…). Ce qui contribue à créer une situation où tous, médecins comme patients, sont amenés à chercher l’explication de toute souffrance là où le réverbère du discours des firmes les éclaire. Le médecin comme les patients sont entraînés par le discours qui les entoure à définir la problématique en termes convergents, avec comme résultat la prescription d’un médicament. Ce qui semble satisfaire toutes les parties mais pose manifestement des problèmes en matière de santé publique. Néanmoins, les firmes pharmaceutiques ne sont pas à elles seules responsables de cette dérive. Elles ne font que suivre une logique marchande, proposent une réponse simpliste à une demande qui existe bel et bien et limitent leurs prises de risques. Elles vont à la rencontre des patients et des médecins pour identifier à la fois des problèmes qui n’ont pas encore trouvé de réponse pharmaceutique et les caractéristiques idéales du produit qui aura le plus de chance de devenir un gros succès commercial. Ces techniques commerciales sont appelées disease mongering dans le monde anglo-saxon9. Que se passe-t-il du côté des patients ? Quel que soit le diagnostic retenu, quelle que soit la personne concernée, la souffrance liée à la condition humaine a toujours été présente et doit être reconnue. Les patients qui se présentent à nous, médecins généralistes ou psychiatres, ne sont pas des malades imaginaires. De nombreuses et passionnantes théories explicatives nous permettent de réactualiser sans cesse notre compréhension des origines du mal-être dans nos sociétés10. Les patients arrivent dans les consultations avec une forte demande de soulagement à laquelle le médecin apporte souvent une réponse médicamenteuse, que ce soit à contrecoeur ou avec conviction. Cette pratique s’est fortement amplifiée depuis l’arrivée sur le marché dans les années 80 d’« antidépresseurs » plus faciles à utiliser (inhibiteurs sélectifs de la recapture de la sérotonine – ISRS) et va encore s’aggraver dans les années à venir avec les nouveaux neuroleptiques ou les anticonvulsivants et la forte incitation à leur prescription dans et en dehors des indications reconnues (« off-label »). D’autres axes de réflexions pourraient être explorés pour comprendre la situation, comme les questions sur la meilleure façon de s’accorder sur des diagnostics psychiatriques et leur degré de pertinence11 ainsi que celles de l’aspect infiniment fuyant et mouvant dans le temps des classifications nosologiques12. Ceux que cela intéresse, se réfèreront à la bibliographie annexée. La complexité est extrême dans l’analyse de ce problème où tous les intervenants portent leur part de responsabilités. Ceci est particulièrement vrai en médecine dans le champ psychiatrique, « science hypermolle » dépourvue de critères objectifs d’évaluation et dans laquelle il faut une dose certaine de naïveté pour oser affirmer une quelconque certitude. Pour comprendre ces incohérences et en suivant un autre parcours explicatif, nous allons essayer de comprendre comment a pu historiquement s’organiser le dérapage actuel dans les pays occidentaux en ce qui concerne la prescription des psychotropes. Nous allons nous pencher sur deux apparitions majeures dans la régulation du médicament au XXème siècle : l’autorisation de mise sur le marché (AMM) et l’essai clinique randomisé en double aveugle (randomized control trials RCT). Autorisation de mise sur le marché (AMM) Peu après l’arrivée des médicaments psychotropes dans les années 60, on a assisté à la mise en place de l’autorisation de mise sur le marché, un mécanisme de contrôle d’abord motivé par l’urgence de protéger le consommateur des produits pharmaceutiques à l’utilité ou à la sécurité douteuse (suite notamment au scandale thalidomide en Allemagne). Et c’est également à ce moment-là, coïncidence historique, que se formait un Marché commun européen, du médicament notamment. En matière de produits pharmaceutiques, les questions de santé publique et économiques sont donc d’emblée indissociables. Les dispositifs de régulation vont se construire en même temps des deux côtés de l’Atlantique et se développent chez nous tant au niveau national qu’européen pour aboutir en 1995 à la création de l’Agence européenne du médicament (European Medicines Evaluation Agency) correspondant de la célèbre Food and Drugs Administration- FDA aux Etats-Unis. La mise en place de l’autorisation de mise sur le marché va nécessiter l’élaboration de critères d’évaluation reproductibles d’un pays à l’autre et une standardisation des pratiques. Il s’agit de garantir à la fois le bénéfice, l’efficacité, la sécurité et la qualité d’une thérapeutique. Le terme thérapeutique est ici essentiel parce qu’il n’est pas question de demander la mise sur le marché d’une substance assurant du mieux-être ou du bien-être et qui s’apparenterait donc à une drogue, à un produit qui permet d’améliorer des performances normales. À la fin des années 60 en effet, la firme Sandoz tenta de commercialiser un nouveau tranquillisant, le Serentil®, en affichant clairement la cible de ce nouveau marché : « le nouveau voisin qui a du mal à se faire des amis dans le quartier, le directeur qui n’arrive pas à s’adapter dans sa nouvelle fonction, la femme qui ne s’entend pas avec sa belle-fille,… ». Serentil® allait aider « les personnes qui répondaient aux situations nouvelles avec un excès d’anxiété ». Le slogan était : « Pour l’anxiété engendrée par une difficulté d’adaptation ». La publicité fut un échec et la Food and Drugs Administration demanda au laboratoire Sandoz de retirer son produit. L’erreur ne fut pas de proposer un remède médical à un problème de société mais de le dire de façon si explicite. Sandoz n’avait pas essayé de redéfinir les problèmes de société en termes de pathologie médicale et de jargon scientifique médical mais avait simplement dit « si vous êtes tendu, voilà un truc qui va vous soulager et vous aider à passer le cap ». Voilà un discours, qui n’étant pas scientifique, était et reste inacceptable13. Pour obtenir l’ouverture d’un marché, et d’autant plus si l’on vise l’obtention d’un remboursement par les assurances et les mutuelles, il faut prouver que l’on vend un médicament et que l’on soigne une maladie. On voit déjà comment à elle seule, cette mesure qui vise à protéger le consommateur va reconfigurer complètement le discours de la médecine et de la psychiatrie. Les études cliniques randomisées L’introduction d’un dossier d’autorisation de mise sur le marché exige de la part des industriels la production d’études fiables, selon le modèle des Randomised control trials créés aux Etats-Unis et au Royaume-Uni. Il s’agit de tester sur une cohorte divisée en deux groupes comprenant de nombreux patients atteints de la pathologie, sur les uns la substance active et sur les autres un placebo ou un médicament de référence plus ancien. L’instauration des Randomised control trials comme prétendus « instruments de connaissance », appliquant la méthode expérimentale à la pratique clinique, va, à partir des années 80 notamment, obliger les psychiatres, dans le monde entier, à recourir à un outil diagnostic universel commun (Diagnostic and Statistical Manuel of Mental Disorders -DSM) qui va profondément modi fier et appauvrir l’élaboration de la clinique psychiatrique. Malgré leur faiblesse méthodologique14, les Randomised control trials ont aujourd’hui un impact considérable sur le développement de la connaissance médicale, la formation des élites scientifiques, l’élaboration des recommandations de prescription. Elles sont par ailleurs l’unique vecteur d’échanges d’informations entre les firmes et les cliniciens. Enfin en donnant une base uniquement statistique au savoir thérapeutique, l’ancienne méthode de construction du savoir clinique, c’est-à-dire l’étude de cas cliniques est complètement tombée en désuétude. Les cliniciens travaillant dans le cadre de ces études passent en général plus de temps à rédiger des protocoles de recherche qu’à proposer une réflexion clinique sur leurs patients. Le style d’interviews utilisés dans ces études, c’est-à-dire le remplissage d’échelles de scores ayant une allure « scientifique », a tendance à s’étendre à la pratique psychiatrique clinique. Les entretiens directifs deviennent la règle en appauvrissant considérablement la relation au patient et sont responsables d’une perte d’informations cruciales sur l’environnement et l’histoire du patient. Soumises à une logique marchande, les firmes conçoivent les Randomised control trials dans l’unique but de mettre en évidence les avantages (plus qu’incertain : me-too) d’un nouveau produit par rapport aux anciens ou hésitent à prendre le risque d’une étude supplémentaire qui accentuerait la mise en évidence d’effets indésirables (nouveaux neuroleptiques et troubles métaboliques ; antidépresseurs inhibiteurs sélectifs de la recapture de la sérotonine et suicide). Ces effets négatifs ne deviendront apparents qu’avec les résultats des études postautorisation de mise sur le marché ou par les premiers signaux apparaissant via la pharmacovigilance. Ainsi, nous voyons actuellement proliférer les indications reconnues et les indications « off-label » pour des nouveaux antipsychotiques dont on sait qu’ils ne présentent pas d’avantages thérapeutiques réels par rapport aux anciens mais qu’ils ont un profil d’effets indésirables comportant davantage de risques. Les sociétés de recherches privées (Contract Research Organizations – CROs) Les Randomised control trials sont des études très coûteuses et pour cette raison ne peuvent être le plus souvent réalisées que par des firmes pharmaceutiques. Celles-ci sous-traitent pour près de 2/3 des études la réalisation de ces recherches à des sociétés privées (Contract Research Organizations – CROs) plutôt qu’à des centres académiques. Ensemble, elles en fixent seules les règles méthodologiques avant de s’assurer la participation de psychiatres cliniciens qui ont beaucoup à y gagner financièrement et en termes de notoriété. Cette nouvelle pratique de la recherche a complètement remodelé les règles de confidentialité, de publication et de propriété intellectuelle en matière de recherche scientifique. Les CROs ont déplacé, probablement pour limiter les coûts, la réalisation des études cliniques dans d’autres régions du globe (Europe de l’Est, Asie, Afrique). Cette nouvelle donne pose des questions non seulement sur le contrôle du recrutement des patients (faux patients, diagnostics erronés,…) mais aussi sur la validité des règles de bonnes pratiques (guidelines) européennes qui sont basées sur des études cliniques randomisées, réalisées de la sorte dans d’autres coins du monde sur des troubles mentaux importés de toutes pièces. Pourtant, l’absence d’universalité des troubles psychiatriques apparaît comme une évidence pour les anthropologues et pour toute personne dotée de bon sens. Que peuvent bien signifier les résultats d’une étude portant sur une cohorte d’enfants diagnostiqués bipolaires en Ossétie du Nord15 pour éclairer notre pratique locale ? Ceci d’autant plus que le diagnostic de bipolarité chez les enfants n’est pas encore établi, ou plutôt commercialisé, en dehors des Etats-Unis. L’effet des médicaments n’est de surcroît pas reproductible d’un coin du globe à l’autre. Par exemple dans les études sur les inhibiteurs sélectifs de la recapture de la sérotonine au Japon, on trouve un effet indésirable que l’on ne retrouve pas ailleurs : la gynécomastie. Pas de généralisation possible non plus du côté de l’appréciation des effets recherchés par le public : les inhibiteurs sélectifs de la recapture de la sérotonine, et en particulier la paroxétine qui a un effet désinhibiteur et qui est utilisée pour le traitement de la « phobie sociale », sont par exemple très mal supportés au Japon. Dans la mentalité japonaise, être désinhibé provoquerait en effet une honte certaine chez un sujet car par un écart de comportement, il risquerait d’offenser gravement son interlocuteur16. Transparence des données des études cliniques Vu les enjeux économiques majeurs et la concurrence acharnée, les firmes gardent la maîtrise du contenu de ces études et le traitement des données statistiques. La firme produit, sans négociation avec les cliniciens, le rapport final sur l’efficacité, la sécurité, les effets secondaires et les recommandations de dosage. La grande majorité des études de phase IV17 ne sont pas soumises aux agences de régulation (Food and Drugs Administration, European Medicines Evaluation Agency). Ne seront publiées que celles de ces études qui montrent un bénéfice du médicament produit par la firme. Vu les enjeux financiers colossaux, il est démontré que les données brutes de ces études ont parfois été rapportées de façon tronquée18,19. De même l’interprétation de la signifiance statistique semble être présentée de manière à maximaliser les bénéfices et à minimiser les risques. Les résultats de ces études restent la propriété des firmes et les détails des données brutes des études, publiées ou non, ne sont pas accessibles à l’analyse des scientifiques indépendants20. Que dire d’une recherche scientifique qui refuse de soumettre ses protocoles et ses résultats à la critique d’autres chercheurs ? Par exemple, la firme pharmaceutique produisant la sertraline n’a finalement obtenu des résultats positifs que dans une étude sur les quatre réalisées et uniquement sur une cohorte comprenant 76% des femmes. Les résultats des études qui montrent un bénéfice sont repris dans des articles scientifiques rédigés par des agences spécialisées (ghostwritting) et sont ensuite attribués et signés par des personnalités académiques, « experts scientifiques » ou « leaders d’opinion », avant d’être publiés dans des revues scientifiques de référence. Les refus de collaboration ou les conséquences scientifiques de négociations déséquilibrées entre industriels et chercheurs qui souhaitent rester indépendants, ne font que très rarement la une des revues médicales. Ceci montre que les stratégies commerciales sont progressivement parvenues à restreindre, dans l’indifférence générale et avec la mise en place d’un cadre légal favorable, le processus normal de recherche. Cas particulier des antidépresseurs La situation actuelle de la pathologie mentale est paradoxale. Il peut être utile de revenir plus en détail au cas des antidépresseurs. La dépression, terme qui désigne une douleur morale qui peut frapper nombreux d’entre nous, est largement décrite et médiatisée. Des campagnes successives nous incitent à y prêter plus d’attention et à être plus interventionnistes dans toute forme de traitement. Et étrangement, dans cette circonstance comme dans d’autres qui touchent à la pathologie mentale, il semble que la qualité de nos traitements soit en net recul21,22,23. Plusieurs méta-analyses de grande ampleur24 concluent que sur tous les patients inclus dans des études cliniques sur l’efficacité des antidépresseurs, seuls 50% des patients connaissent une amélioration clinique mesurable sur l’échelle d’Hamilton. Ce qui est un résultat assez médiocre comparativement aux 40% d’amélioration sous placebo.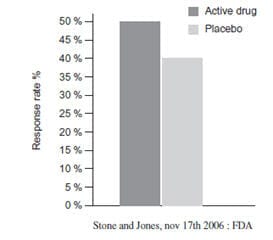 Ainsi, si nous regardons 10 patients traités, 5
patients seulement connaissent une amélioration grâce aux médicaments. Mais parmi
ceux-ci, 4 répondraient de toute façon à un
placebo. Seul 1 patient sur 10 ne répond donc
spécifiquement qu’au médicament testé.
La différence même minime entre les effets de
la substance active et le placebo, mais « statistiquement significative » est considérée comme
suffisante pour attester que le médicament
« fonctionne ». Les agences de régulation approuvent ces drogues et les firmes en font la
promotion comme s’il s’agissait de vrais traitements d’une maladie. Ensuite, les cliniciens les
prescrivent abondement. Si cette constatation
théorique sur l’effet placebo était utilisée dans
la pratique clinique, il devrait y avoir un plus
grand usage de placebo ou à tout le moins, une
attente prudente avant de prescrire des médicaments. En cas de réponse positive, le clinicien
devrait informer le patient du fait que l’amélioration pourrait être induite par d’autres facteurs.
Ou encore, il devrait être possible d’optimaliser
ces autres facteurs pour arriver pratiquement
au même résultat que les substances qui
« fonctionnent » et donc éviter les effets indésirables et les risques non négligeables25 qu’occasionnent les substances actives.
En y regardant de plus près sur des études
englobant un très grand nombre de patients,
même une petite différence d’un ou deux points
sur une échelle peut donner une différence
« statistiquement significative ». Ce qui veut
dire qu’une substance qui est soit un peu sédative soit un peu calmante donne des résultats
positifs pour « soigner la dépression » si l’échelle de scores utilisée pour mesurer l’efficacité
inclut des items tels que la qualité du sommeil
ou l’anxiété. De cette façon, il serait possible
de prouver que la nicotine, les benzodiazépines,
les antihistaminiques, le méthylphénidate, les
antipsychotiques et la plupart des anticonvulsivants sont des « antidépresseurs ». La plupart
de ces produits ont d’ailleurs déjà montré leur
efficacité dans des Randomised control trials.
Les patients qui reçoivent un « antidépresseur »
ont 50% de chance de ne pas ressentir d’effet
bénéfique et 50% de chance de ressentir un effet
peut-être un peu plus bénéfique ou peut-être
simplement comparable qu’avec de la nicotine
ou un antihistaminique par exemple. Il ne s’agit
donc certainement pas d’un traitement spécifique « magic bullet ». Pourtant, le patient sera
convaincu par différentes sources d’information sur les antidépresseurs de recevoir un
médicament à l’effet équivalent sur son
mal-être que l’effet d’un antibiotique sur
une pneumonie ou de l’insuline pour le
diabète.
Ainsi, si nous regardons 10 patients traités, 5
patients seulement connaissent une amélioration grâce aux médicaments. Mais parmi
ceux-ci, 4 répondraient de toute façon à un
placebo. Seul 1 patient sur 10 ne répond donc
spécifiquement qu’au médicament testé.
La différence même minime entre les effets de
la substance active et le placebo, mais « statistiquement significative » est considérée comme
suffisante pour attester que le médicament
« fonctionne ». Les agences de régulation approuvent ces drogues et les firmes en font la
promotion comme s’il s’agissait de vrais traitements d’une maladie. Ensuite, les cliniciens les
prescrivent abondement. Si cette constatation
théorique sur l’effet placebo était utilisée dans
la pratique clinique, il devrait y avoir un plus
grand usage de placebo ou à tout le moins, une
attente prudente avant de prescrire des médicaments. En cas de réponse positive, le clinicien
devrait informer le patient du fait que l’amélioration pourrait être induite par d’autres facteurs.
Ou encore, il devrait être possible d’optimaliser
ces autres facteurs pour arriver pratiquement
au même résultat que les substances qui
« fonctionnent » et donc éviter les effets indésirables et les risques non négligeables25 qu’occasionnent les substances actives.
En y regardant de plus près sur des études
englobant un très grand nombre de patients,
même une petite différence d’un ou deux points
sur une échelle peut donner une différence
« statistiquement significative ». Ce qui veut
dire qu’une substance qui est soit un peu sédative soit un peu calmante donne des résultats
positifs pour « soigner la dépression » si l’échelle de scores utilisée pour mesurer l’efficacité
inclut des items tels que la qualité du sommeil
ou l’anxiété. De cette façon, il serait possible
de prouver que la nicotine, les benzodiazépines,
les antihistaminiques, le méthylphénidate, les
antipsychotiques et la plupart des anticonvulsivants sont des « antidépresseurs ». La plupart
de ces produits ont d’ailleurs déjà montré leur
efficacité dans des Randomised control trials.
Les patients qui reçoivent un « antidépresseur »
ont 50% de chance de ne pas ressentir d’effet
bénéfique et 50% de chance de ressentir un effet
peut-être un peu plus bénéfique ou peut-être
simplement comparable qu’avec de la nicotine
ou un antihistaminique par exemple. Il ne s’agit
donc certainement pas d’un traitement spécifique « magic bullet ». Pourtant, le patient sera
convaincu par différentes sources d’information sur les antidépresseurs de recevoir un
médicament à l’effet équivalent sur son
mal-être que l’effet d’un antibiotique sur
une pneumonie ou de l’insuline pour le
diabète.
Du diagnostic raffiné au diagnostic plat « Je ne veux pas cacher que certaines évolutions me préoccupent et je voudrais à ce sujet récapituler mon avis concernant l’appauvrissement du diagnostic psychiatrique et de son traitement. Le diagnostic psychiatrique était au siècle passé et jusqu’aux années 80, il est vrai, peu fiable et valide, mais il était raffiné. Ce raffinement était dû à la phénoménologie et à la psychanalyse, en ce temps-la deux mouvements dominants de la psychiatrie, du moins en Europe occidentale. Le diagnostic psychiatrique est devenu « plat », a perdu de sa richesse et s’est desséché… L’être individuel, tant dans ses manifestations normales que dans celles éventuellement pathologiques, demeure en majeure partie un livre clos lorsqu’il est détaché de son passé….La personnalité ne peut être assimilée au cerveau. Ne pas tenir compte du passé , de l’analyse du passé ou de la structure de la personnalité sont, sur le plan diagnostique, des fautes médicales….Un manque d’intérêt (pour la psychodynamique) mène à peu de recherche. Peu de recherches mènent (depuis quelques décennies) au mépris de notre profession… Il est clair pour chaque clinicien que, d’une part, une amélioration substantielle peut être obtenue avec des psychotropes, mais que d’autre part, une partie des patients ainsi traités ne s’améliore pas ou insuffisamment. Ceci concerne dans le cas de la maladie dépressive plus de la moitié des patients… Les tentatives de suicide et les suicides réussis, complications les plus inquiétantes de la maladie dépressive, n’ont qu’à peine diminué durant l’ère des antidépresseurs. La cause de cette déterioration n’est pas claire. Il me semble qu’y contribuent des facteurs tels que : • la surestimation des déterminants biologiques des dépres sions et donc du traitement psychopharmacologique et • la sous-estimation du fait que des fondements neurobiologiques de la dépression peuvent être (co-)induits par des facteurs psychologiques et psychodynamiques une attitude qui mène facilement à la marginalisation de la psychothérapie et à la prescription d’antidépresseurs en monothérapie- ont contribué à cette situation décevante. Tout compte fait, nous avons payé un prix élevé pour l’innovation diagnostique telle qu’elle a été instaurée en 1980… ». Extraits de la préface rédigée par le Pr H.M. VAN PRAAG H.M. : 2003 de DIERICK M, ANSSEAU M, D’HAENEN H, PEUSKENS J, LINKOWSKI P. (Eds). Manuel de Psychopharmacothérapie. Gent, Academia Press, 2003, 678 p.L’utilisation massive des Randomised control trials ne permet pas d’étayer l’observation clinique fine qui nous apprend que certaines drogues aident certaines personnes mais d’autres pas. Plus inquiétant encore, les patients qui se sentaient bien sous benzodiazépines ou d’anciens psychotropes ont été fortement incités à se sevrer pour prendre un inhibiteur sélectif de la recapture de la sérotonine qui ne leur fait aucun effet. La différence majeure entre ces différentes drogues plus anciennes et les médicaments qui sont qualifiés d’« antidépresseurs » est que ces derniers ont reçu une autorisation de mise sur le marché et ont bénéficié d’une promotion agressive et efficace pour le traitement de la dépression. De leur côté, la nicotine ou les antihistaminiques (trop connus pour d’autres usages) n’auraient pas été commercialisés de façon crédible pour cette indication tandis que les antipsychotiques et les anticonvulsivants sont orientés vers d’autres cibles commerciales (troubles de l’humeur,…). En cours de route, d’autres médicaments tout aussi utiles dans le traitement de symptômes dépressifs ont vu leur utilisation marginalisée (par exemple les tricycliques ou les benzodiazépines). Contrairement aux études réalisées dans les autres champs de la médecine, les études randomisées concernant les psychotropes n’apportent pas de preuves que ces médicaments sauvent des vies ou permettent de remettre des gens au travail. Tout au plus, ces études montrent que ces substances ont un effet, « fonctionnent » chez certaines personnes. Mais avoir un effet ne veut pas dire qu’il s’agit d’un traitement efficace. Cette efficacité spécifique reste à prouver (par exemple, un effet sédatif avéré n’est pas une preuve d’efficacité sur les symptômes dépressifs). La psychiatrie basée sur les preuves et les règles de bonnes pratiques (guidelines) Une fois établies « les preuves » de l’efficacité des psychotropes via les Randomised control trials, l’étape suivante est de s’assurer que les cliniciens adhèrent aux règles de bonnes pratiques en matière de prescription (guidelines) synthétisées par un groupe d’experts. Les gestionnaires de soins attendent ensuite des cliniciens qu’ils suivent ces guidelines. Toute déviation par rapport à celles-ci de la part d’un clinicien implique de pouvoir être justifiée, ce qui transforme peu à peu et sans légitimité, ces lignes de conduite en règles contraignantes. Le clinicien est fortement incité à traiter ses patients non pas d’après sa longue expérience clinique ou les études de cas rédigées par ses pairs mais d’après des études statistiques dont la méthodologie semble souvent douteuse. Nous ne disposons actuellement d’aucune alternative aux Randomised control trials pour rédiger ces guidelines.
Détérioration
Cette détérioration qui transparaît au travers de tout ce qui a déjà été dit ici ressort nettement dans plusieurs études menées par Healy et Al sur la population d’un hôpital psychiatrique du Nord du Pays de Galles26,27. En 50 ans, les mesures d’internement forcé en psychiatrie ont été multipliées par 5 ; les admissions pour pathologies mentales sévères, par 7 ; le taux de suicide chez les patients schizophrènes par 20 et la mortalité générale pour les malades atteints de pathologies psychiatriques sévères a fortement augmenté. Ces résultats se retrouvent dans des études faites dans d’autres pays et semblent corrélés avec la quantité de psychotropes prescrites.Conclusion
Nous voyons donc qu’actuellement le savoir psychiatrique, celui qui est partagé par les médecins comme celui qui est diffusé dans le grand public, est orienté par la nécessité pour les firmes d’obtenir ces autorisations de mise sur le marché et par des contraintes de marketing : état du marché, concurrence, évolution des besoins, habitudes de prescription, … La question de l’objectivité de la recherche biomédicale nécessite un débat beaucoup plus vaste sur les rapports de pouvoir qui structurent ce secteur, sur les mécanismes de sélection des projets, sur le statut de la recherche postautorisation de mise sur le marché et finalement sur le rôle de la puissance publique dans le processus d’innovation en matière de médicament. Le combat pour la transparence reste primordial. Les données brutes des Randomised control trials devraient être soumises à l’interprétation critique par d’autres chercheurs, tant pour ce qui concerne les données des études montrant un bénéfice que pour celles qui ne donnent pas de résultats favorables. De façon tout à fait évidente, les Randomised control trials ne sont pas construites pour orienter la pratique clinique. Si c’était le cas, elles devraient s’intéresser plus largement à tout le processus de soins dans lequel le médicament n’est qu’un élément marginal. De façon plus générale, c’est toute une logique de type marchande qui met à son service les soignants, en réduisant la pratique des soins à l’échange d’un produit de consommation, clairement délimité, et en élaguant de ce fait tout ce qui n’entre pas dans ce cadre et principalement le rapport humain et l’engagement dans la durée auprès des patients28. Notre objectivité nous oblige à prendre en compte la subjectivité des patients comme une donnée irréductible qui ne relève en rien d’une vision passéiste de la psychiatrie.Documents joints
- HEALY D., The Creation of Psychopharmacology, Cambridge, Massachussets, London, England, Harvard University Press. 2002, 469 p.
- URFALINO P., HAURAY B., « Expertise scientifique et intérêts nationaux. L’évaluation européenne des médicaments 1965-2000 », Revues Annales. Histoire, Sciences sociales, 2007, n°2, Médicaments et Société.
- VALENSTEIN E., Blaming the Brain – The Truth About Drugs and Mental Health, New York, The Free Press, 1998, 292 p.
- F. Gonon déclare « Nous sommes quelques neurobiologistes spécialistes de la dopamine. Nous craignons que les recherches récentes ne soient utilisées pour justifier « scientifiquement » une médicalisation de la difficulté de vivre », GONON F et GIROUX-GONON., Université Bordeaux 2, « Neurosciences et traitement médicamenteux de la souffrance psychique », http ://www.vivagora.org/ article.php3 ?id_article=109.
- BOUTSEN M., LAASMAN J.-M., REGINSTER N., Données socio-économiques et étude longitudinale de la prescription des antidépresseurs, Mutualité socialiste de Belgique, 2006.
- BRIOT M., Députée, Rapport sur le bon usage des médicaments psychotropes – Synthèse générale, Office parlementaire d’évaluation des politiques de santé, 2006, http ://www.psy-desir.com/leg/spip.php ?article1451.
- Communiqué de presse n°4 du 1er mars 2007 « L’abus de médicaments délivrés sur ordonnance va dépasser la consommation de drogues illicites, indique l’OICS », OICS, http ://www.incb.org/incb/ fr/press_releases.html.
- VANDEREYCKEN W., VAN DETH R., Psychiaters te koop, Antwerpen, Garant, Cyclus, 2006, 272 p. ; ANGELL M., The Truth About The Drug Companies – How they Deceive Us and What About To Do About It, New York, Ed.Random House Trade Paperbacks, 2005, 319 p.
- MINTZES B. « Disease Mongering in Drug Promotion : Do Governement Have a Regulatory Role », PLOS Medicine, avril 2006, http :// medicine.plosjournals.org.
- EHRENBERG A. La fatigue d’être soi – Dépression et société, Paris, Odile Jacob, 1998, 414 p. ; PIGNARRE Ph., Comment la dépression est devenue une épidémie, Paris, Hachette, 2003, 153 p ; ELIOTT C., Better Than Well – American Medecine Meets The American Dream, New York, London, W.W.Norton & Company, 2003, 357 p.
- KIRK S., KUTCHINS H., Aimez-vous le DSM : le triomphe de la psychiatrie américaine, Le Plessis- Robinson, Institut Synthélabo, Coll. Les Empêcheurs de Penser en Rond, 1998, 424 p.
- HACKING I., L’âme réécrite – Etude sur la personnalité multiple et les sciences de la mémoire, Paris, Les Empêcheurs de Penser en Rond, 2006, 451 p.
- ELIOTT C., Better Than Well – American Medecine Meets The American Dream, New York, London, W.W.Norton & Company, 2003, 357 p.
- « Progrès thérapeutique : la faillite des agences » et « Les agences du médicament n’exigent pas assez d’évaluations comparatives », Prescrire, décembre 2002, n° 234, p. 847 et p. 850 et 851.
- Voir pour plus de détails : http ://www.outclinicaltrials.com.
- ELIOTT C., Better Than Well – American Medecine Meets The American Dream, New York, London, W.W.Norton & Company, 2003, 357 p.
- Pour bien comprendre le déroulement complet des recherches autour du médicament : URFALINO P., Le grand méchant loup pharmaceutique : angoisse ou vigilance, Paris, Textuel, Conversation pour demain, 2005, 119 p.
- URFALINO P., HAURAY B., « Expertise scientifique et intérêts nationaux. L’évaluation européenne des médicaments 1965-2000 », Revues Annales. Histoire, Sciences sociales, 2007, n°2, Médicaments et Société.
- DALGARRONDO S., « Savoir thérapeutique et logique commerciale. Le cas de l’AZT », Revues Annales. Histoire, Sciences sociales, 2007, n°2, Médicaments et Société.
- HEALY D., Trussed in evidence : guidelines, tramlines and fault lines. Texte de la présentation Pills, Politics and Practice Demanding People- Centred Medicines Policy in the 21st Century October 26-27 2006, Amsterdam. HAI Europe Jubilee Conference.
- COUPECHOUX P., Un monde de fou : comment notre société maltraite ses malades mentaux. Paris, Seuil, 2006. 358 p.
- HEALY D, HARRIS M, CATELL D et AL (2005). Service utilisation in 1896 and 1996 : morbidity and mortality data from North wales, Hist Psychiatrica 16,27-41.
- HEALY D, HARRIS M, TRANTER R et Al (2006). Lifetime suicide rates in treated schizophrénia : 1875-1924 and 1994-1998 cohorts compared, British J Psychiatry 188, 223-228.
- HEALY D., Trussed in evidence : guidelines, tramlines and fault lines. Texte de la présentation Pills, Politics and Practice Demanding People- Centred Medicines Policy in the 21st Century October 26-27 2006, Amsterdam. HAI Europe Jubilee Conference.
- MIGNOT G., Effets indésirables des antidépresseurs . Texte de la présentation à la réunion de consensus sur l’usage efficient des antidépresseurs dans le traitement d’indications autres que les troubles dépressifs. INAMI. Bruxelles, 31 mai 2007.
- HEALY D, HARRIS M, CATELL D et AL (2005). Service utilisation in 1896 and 1996 : morbidity and mortality data from North wales, Hist Psychiatrica 16,27-41.
- HEALY D, HARRIS M, TRANTER R et Al (2006). Lifetime suicide rates in treated schizophrénia : 1875-1924 and 1994-1998 cohorts compared, British J Psychiatry 188, 223-228.
- Mol A., De logica van het Zorgen : Actieve patienten en de grenzen van het kiezen. Amsterdam, Vangennep, 2006. 158p.
Cet article est paru dans la revue:
Santé conjuguée, n° 44 - avril 2008
L’arrivée des psychotropes a bouleversé le paysage de la psychiatrie. Si le bénéfice que l’industrie retire de cette mutation est imposant, celui qui revient aux patients est beaucoup plus incertain… Historique Après la seconde guerre mondiale(…)
Le médicament prend une place de plus en plus considérable dans nos vies. Au- delà du développement scientifique, deux phénomènes concourent à cet es- sor. D’une part, l’efficacité du médica ment est survalorisée alors que ses(…)
La visite des délégués médicaux pose beaucoup de questions. Quelles sont les limites de l’information dispensée par les firmes sur les médicaments ? Quel- les sont les autres possibilités d’accès à l’information tant scientifique qu’administrative ?(…)
Le Centre belge d’Evidence Based Medicine ou CEBAM existe depuis 2001 (www.cebam.be). Sa mission est de promouvoir l’Evidence Based Medi cine en Belgique (voir encadré), c’est- à-dire d’organiser des cours de lecture critique, participer au travail(…)
Des « délégués » ne dépendant pas des firmes et proposant une information objective Evidence Based Medicine… le croiriez-vous ?
Qui parle aux étudiants en médecine des firmes pharmaceutiques ? Person- ne ! Et pourtant, chaque médecin est confronté à ces acteurs fondamentaux du monde de la santé. Grâce à la recherche qu’elles soutiennent et aux(…)
Les dérives du monde pharmaceutique ne sont pas une fatalité. Il est possible de développer un esprit critique et de réagir. Illustration par le Groupe de recherche et d’action pour la santé, GRAS, constitué de praticiens(…)
Sans oublier les revues périodiques et les sites recommandés au fil des pages du cahier, voici quelques lectures passionnantes. Les inventeurs de maladie, Manoeuvres et manipulations de l’industrie pharmaceutique, Jörg Blech, Actes Sud 2005. « Si(…)

